Lactobacilos para niños: Refuerza sistema inmunológico
FUNCIÓN INMUNITARIA DE LOS PROBIOTICOS
El aumento de las enfermedades alérgicas en la niñez es un problema que ha ido en aumento en los últimos años. Se estima que la dieta moderna contiene menos bacterias que las dietas pasadas. La "hipótesis de la higiene" sugiere que la disminución en la exposición a microbios que estimulan el sistema inmune durante la infancia temprana es una explicación para el incremento en la prevalencia de las alergias y asma. La exposición microbiana es la señal ambiental más fuerte para la maduración postnatal del sistema inmune, además de inducir maduración de las células presentadoras de antígenos y de las células T regulatorias que son esenciales para la programación y regulación de las respuestas de células T. Actualmente se tiene evidencia de que ciertas cadenas de lactobacilos y bifidobacterias pueden influenciar la respuesta inmune mediante diferentes vías. La microbiota intestinal tiene efecto anti-inflamatorio a nivel local.
Bjorksten y sus colegas descubrieron que hay una diferencia en la colonización de bacterias entre niños alérgicos y no alérgicos. Los infantes alérgicos de 2 años tienen una menor presencia de lactobacilos en comparación con los no alérgicos, mientras que los no alérgicos presentan un mayor número de coliformes y Staphylococcus aureus.
En estudios más recientes, se ha encontrado que los niños alérgicos presentan colonización de especies de bifidobacterias que son más comunes en adultos. La dermatitis atópica asociada a la alergia a la proteína de la leche de vaca en la infancia fue evaluada usando formula a base de hidrolizados con y sin probiótico LGG, aquellos que recibieron formula con probiótico mostraron mejoría significativa en la clasificación clínica de eczema, así como, cambios en los marcadores de inflamación intestinal. Se ha demostrado que LGG administrado junto con una dieta de eliminación a niños con dermatitis atópica a causa de alergia a leche de vaca, disminuyen IL4 e incrementan interferón, dirigiendo el sistema inmune a disminuir la inflamación.
Se sugiere que su uso sea dirigido a los pacientes en la edad temprana antes de que la enfermedad alérgica se haya establecido. LGG fue administrado a mujeres embarazadas y a sus hijos hasta los 6 meses de edad quienes contaban con historia familiar de alergia demostrándose diferencia significativa en el desarrollo de eczema en el grupo tratada hasta los 2 años de edad.
PARTO MATERNO
El proceso de colonización del intestino del lactante por bacterias comienza pocas horas después del parto. Este proceso es fundamental para el desarrollo del sistema inmunológico posnatal. La respuesta inmunitaria a las bacterias intestinales se inicia en las primeras horas de vida, que son críticas para el desarrollo de la microbiota intestinal. Esta última tiene un efecto importante en la función de protección contra enfermedades infecciosas e inmunológicas. El neonato tiene dos oportunidades de exposición a bacterias: el momento del parto y la lactancia. Ambos eventos determinan qué tipo de bacterias colonizarán el intestino del neonato.
Las bifidobacterias son uno de los grupos bacterianos más importantes en la microbiota infantil y se han asociado con una microbiota intestinal "saludable". Esto se debe a que predominan en la microbiota de lactantes alimentados con leche materna en comparación con los que reciben fórmula infantil, en los cuales no hay un predominio de bifidobacterias. Además de la lactancia materna, otros factores que influyen en la composición de la microbiota del lactante son el tipo de parto (vaginal versus cesárea), la administración de antibióticos en las primeras etapas de vida, así como también el entorno y la higiene en el que se desenvuelve el lactante.
El parto vaginal no se considera un proceso estéril, a diferencia del parto por cesárea. Durante el nacimiento a través del canal vaginal, el recién nacido es expuesto a bacterias que forman su primer "inóculo" oral y algunas de ellas se establecerán en su intestino.
Los lactantes nacidos por cesárea tienen una microbiota desprovista debifidobacterias, y más a menudo se colonizan con C. difficile, a comparación de aquellos nacidos por parto vaginal, que tienen una microbiota rica en bifidobacterias y lactobacilos. Estos patrones de colonización persisten por muchos meses. A su vez, la tasa de alergias y asma es mayor en individuos nacidos por cesárea, con poca colonización por bifidobacterias, comparada con aquellos nacidos por parto vaginal.
LACTANCIA MATERNA
La lactancia materna no es un proceso aséptico y la leche humana no es un fluido estéril. La leche materna contiene una cantidad importante de bacterias, entre ellas algunas cepas de lactobacilos como L. reuteri, L. plantarum y L. salivarium. Estudios recientes han confirmado la abundancia del género de Bifidobacterium en leche humana, hallándose en hasta 85-100% de las muestras obtenidas. Algunas de las especies identificadas son aquellas con propiedades de probióticas, incluyendo B. adolescentis, B. animalis, B. breve, B. bifidum, B. cantenalatum, B. longum. Se ha reportado que la leche humana contiene una concentración de bifidobacterias de 1 × 103 unidades formadoras de colonias.
Independientemente de los mecanismos involucrados, con la alimentación a pecho, a partir de la primera semana de vida, el lactante desarrolla una microbiota intestinal rica en bifidobacterias. Los lactantes alimentados con fórmulas desarrollan una microbiota diferente, menos diversa, sin predominio de bifidobacterias, y mayores cantidades de bacteroides, Clostridium y enterobacteria
Es fundamental tomar en cuenta que los bebés que son alimentados con leche materna reciben constantemente una cantidad de bacterias con cada toma, entre ellas bifidobacterias no patógenas, las cuales contribuyen a estimular la respuesta inmunológica del bebé. En contraste, los bebés que son alimentados con fórmulas, siempre y cuando estas sean preparadas correctamente, no reciben bacterias.
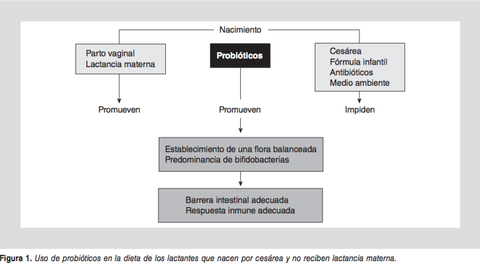
Después del destete, la composición de la microbiota se vuelve más homogénea y menos diferente entre los lactantes amamantados y los que reciben fórmula. En síntesis, la introducción de bacterias en el recién nacido durante el parto y la lactancia natural produce alteraciones en la microbiota del niño, lo que se relaciona con una mayor protección inmunológica y una disminución en el riesgo de padecer enfermedades infecciosas y alérgicas. El parto por cesárea, las fórmulas infantiles sin microbios, los antibióticos y el medio ambiente saneado, si bien protegen al lactante de patógenos, no favorecen el desarrollo de una microbiota «sana», son predominio de bifidobacterias, y, en consecuencia, llevan a un desarrollo inadecuado de protección de la barrera intestinal y una respuesta inmune inadecuada. Estas observaciones proporcionan una sólida base teórica para el uso de bacterias seguras, en la dieta de los lactantes, especialmente en aquellos que nacen por cesárea y no reciben lactancia materna.
PROBIÓTICOS
Los microorganismos probióticos son parte de la dieta y, al ser consumidos, suministran al huésped una mayor cantidad de bacterias de las que normalmente se ingieren en la dieta occidental moderna. Se considera que una bacteria es probiótica cuando se ha demostrado que su consumo tiene efectos clínicos o funcionales beneficiosos para el huésped.
Algunos informes indican que los lactantes pueden mantener los probióticos en su organismo si sus madres recibieron una bacteria específica durante el embarazo. Esto sugiere que existe una oportunidad para que los probióticos se establezcan verdaderamente en el organismo durante la "ventana" de colonización en el período neonatal inmediato. En este caso, los probióticos se ingieren como parte del primer "inóculo" oral de bacterias maternas, junto con las bacterias del canal de parto, de la leche materna y del entorno para formar parte de la "flora natural" o "bacterias residentes" del lactante. La administración oral de Lactobacillus y cepas específicas de Bifidobacterium aumenta la presencia de estas especies en las heces de prematuros, lactantes a término y niños mayores, lo que demuestra su capacidad de colonización en todo el tracto gastrointestinal.
La mayoría de los estudios han centrado su atención en los conteos de bacterias fecales. No obstante, el aumento de ciertas bacterias probióticas en el intestino proximal, que generalmente se encuentra poco colonizado debido a las dietas occidentales, puede ser de igual o mayor importancia en la regulación de la inmunidad intestinal que resulta de las alteraciones en el perfil de bacterias intestinales. Estos efectos pueden ser especialmente relevantes en los recién nacidos, ya que los cambios inmunológicos durante esta etapa pueden tener consecuencias a largo plazo.
MECANISMOS DE ACCIÓN DE BACTERIAS PROBIÓTICAS
Los cambios funcionales documentados con el uso de probióticos explican los efectos clínicos que se mencionan más adelante:
- Aumento de la cantidad de bifidobacterias en comparación con otras especies en prematuros, lactantes a término y niños mayores.
- Reducción de bacteroides, Clostridium y coliformes en las heces.
- Disminución del pH en el interior del intestino, lo que dificulta el crecimiento de patógenos.
- Incremento de producción de mucina (moco) intestinal.
- Activación de macrófagos y capacidad fagocítica.
- Incremento de actividad de linfocitos killer.
- Incremento de niveles de IgA en el lumen intestinal.
- Incremento de células circulantes productoras de IgA, inmunoglobulina M (IgM) e inmunoglobulina G (IgG).
- Disminución de la permeabilidad intestinal.
- Disminución de producción de citocinas asociadas con el proceso inflamatorio (antitripsina fecal, proteína eosinofílica urinaria, factor de necrosis tumoral) y producción de citocinas antiinflamatorias, incluyendo factor de crecimiento transformante β (TGF-β).
Estos mecanismos han sido documentados con el uso de varios probióticos en la función de la barrera intestinal y la respuesta inmune y explican los efectos clínicos en prevención y tratamiento de varias condiciones patológicas específicas demostradas en estudios humanos.
BENEFICIOS CLÍNICOS DE LOS PROBIÓTICOS EN PEDIATRÍA
Los efectos clínicos del uso de probióticos específicos en pediatría se pueden describir de la siguiente manera:
- Cambios en la función del sistema inmunológico relacionados con la protección del organismo, el mantenimiento de la barrera intestinal y la regulación de la respuesta inmunitaria.
- Reducción de riesgo (prevención) de condiciones clínicas específicas (p. ej. enfermedades infecciosas, particularmente diarrea viral, enfermedad atópica, diarrea asociada con antibióticos, enterocolitis necrotizante [ECN]).
- Manejo (terapia) de ciertas condiciones clínicas (p. ej. el manejo de la diarrea viral aguda, enfermedad atópica, y el cólico infantil). Si bien se ha avanzado en el reconocimiento del potencial terapéutico de ciertos probióticos (particularmente en el manejo de diarrea aguda, que se menciona a continuación), el mayor potencial de estos agentes yace en la prevención de problemas como la diarrea o alergia, con el uso regular en poblaciones generales (niños sanos), o en la prevención de enfermedades como ECN, en poblaciones de riesgo (prematuridad).
EFECTOS INMUNOLÓGICOS Y ENFERMEDADES INFECCIOSAS AGUDAS
Los probióticos han sido documentados como efectivos para mejorar la función intestinal y modular la respuesta inmune, gracias a diversos efectos funcionales. Entre ellos se incluyen la modulación positiva de la composición de la microbiota, la competencia con bacterias patógenas por receptores mucosos, el aumento en la producción de IgA secretora y mucina, la producción de sustancias antimicrobianas y la disminución de la permeabilidad intestinal. Estos efectos han sido evidenciados en una amplia gama de estudios sobre la ingesta de probióticos y explican los diversos resultados clínicos obtenidos. Estos incluyen disminución de la excreción viral (en infección por rotavirus), una reducción del riesgo de prevención de enfermedad aguda y disminución en enfermedades respiratorias, y gastrointestinales. Varios de estos estudios también documentan resultados indirectos del mantenimiento de la salud, tales como disminución del ausentismo a colegios y guarderías infantiles, y disminución en el uso de antibióticos en poblaciones pediátricas.
SEGURIDAD DE LOS PROBIÓTICOS EN PEDIATRÍA
El perfil de seguridad, así como la eficacia de un agente probiótico, depende del género, la especie y la cepa específica de las bacterias que se han estudiado. Es importante entender que la «seguridad» de una bacteria se establece principalmente a través de una evaluación completa de las características mismas de esa bacteria.
Una bacteria probiótica debe tener una historial de uso seguro en grandes números de poblaciones o individuos, y, por último, no mostrar efectos indeseables en ensayos clínicos controlados. No hay casos de infecciones por bifidobacterias. Además, no se ha reportado ningún efecto negativo en estudios clínicos con lactantes, incluyendo neonatos, ni en poblaciones vulnerables como prematuros, desnutridos y los lactantes nacidos de madres con VIH. Esto hace que este género de bacterias sea particularmente adecuado para el uso general en lactantes.
El B. lactis es, en la actualidad, la única bacteria probiótica evaluada por la Food and Drug Administration (FDA) con afirmación de ser generally regarded as safe (GRAS) para su uso en recién nacidos sanos en EE.UU.
Lactobacillus, especialmente L. rhamnosus GG, puede considerarse un probiótico más apropiado para el lactante o un niño mayor.
CONCLUSIONES
El consumo de ciertos microbios probióticos con un perfil de seguridad adecuado, en los primeros años de vida, tiene un efecto positivo sobre la función de barrera de intestino y respuesta inmunitaria. El potencial que tienen ciertos probióticos de beneficiar la salud del lactante y la población en general es cada vez más tangible.
En PAVIA encontrarás el FreeTX y OM3, probióticos con la cepa adecuada para ellos que es la L. Rhamnosus y además adicionados con nutrientes especiales, seguros y efectivos para niños con un sabor que les encantará.







